Trifluor -metanszulfonsav, egy nagyon erős szerves sav, CAS 1493-13-6, CF3SO3H molekuláris képlet, színtelen folyadék, sárga vagy sárga-barna folyadék szennyeződésekkel, dohányzik a levegőben. Nagyon oldódó vízben; Könnyen oldódik a poláris szerves oldószerekben, például dimetil -formamidban, acetonitrilben és dimetil -szulfonban. Az oldódási folyamat során az intenzív hőkibocsátás miatt azonban veszélyt és alacsony toxicitást okozhat, ha gyorsan hozzáadják a poláris oldószerhez. Széles körű felhasználási választékkal rendelkezik, és az egyik ismert szupersav. Erős korrózióval és higroszkópossággal rendelkezik, és széles körben használják az orvostudományban, a vegyiparban és más iparágakban. Kis adagolással, erős savassággal és stabil tulajdonságokkal rendelkezik. Cserélheti a hagyományos szervetlen savakat, például a kénsavat és a sósavat, és sok alkalommal játszhat a folyamat optimalizálásában és javításában.

|
Vegyi képlet |
CHF3O3S |
|
Pontos tömeg |
150 |
|
Molekulatömeg |
150 |
|
m/z |
150 (100.0%), 152 (4.5%), 151 (1.1%) |
|
Elemi elemzés |
C, 8.00; H, 0.67; F, 37.98; O, 31.98; S, 21.36 |
|
|
|

Trifluor -metanszulfonsav(TFOH vagy TFMSA), a CF ∝ SO ∝ H kémiai képlettel, egy nagyon savas szerves vegyület, amelynek PKA -értéke -14,7 -es értéke, messze meghaladja a hagyományos szerves savak, például a kénsav és a sósav savasságát. Az erős savasság, a nagy hőstabilitás, az alacsony nukleofilitás és a kiváló oldhatóság egyedülálló kémiai tulajdonságaival nélkülözhetetlen "univerzális katalizátor" és "funkcionális additív" lett a modern vegyiparban.
1. Benchmark reagens a savas katalizált reakciókhoz
Szuperacidként hatékonyan képes katalizálni a különféle savfüggő reakciókat, ideértve az észterációt, az alkilezést, a polimerizációt, a dehidrációt és az izomerizációt. Alapvető előnyei rejlenek:
Nem nukleofil katalízis: A konjugált bázisának (trifluor -metanszulfonát) szinte nincs nukleofilitása, elkerülve a hagyományos savas katalízisben bekövetkezett nukleofil támadások által okozott mellékreakciókat, jelentősen javítva a reakció szelektivitását és a hozamot. Például a Friedel Crafts acilezési reakciójában a trimetil -szilil -észter katalizálhatja az intramolekuláris ciklizációt és hatékonyan szintetizálhatja a ciklikus ketonvegyületeket, amelyek kulcsfontosságú intermedierek az antidepresszáns gyógyszer -fluoxetin előállításához.


Extreme condition adaptability: It can remain stable in high temperature (>200 fok) vagy erősen oxidáló környezet, amely alkalmas magas hőmérsékletű polimerizációs reakciókra vagy oxigéntartalmú vegyületek szintézisére.
Például az etilén -keton oligomerizációjának poliketid polimer anyagokból történő katalizálásának katalizációja jobb hőállóság és mechanikai szilárdsággal rendelkezik, mint a hagyományos polietilén.
Zöld kémiai szubsztitúció: helyettesítheti az erősen szennyező szervetlen savakat (például kénsavat és hidrofluorinsavat), és csökkentheti a hulladéksav -kibocsátást. Például az alkilezési reakcióban az izobután és a butént katalizáló izooktán katalizátora 15% -kal növeli a hozamot, és 60% -kal csökkenti a hulladéksav kezelésének költségeit.
2.
A TFMSA és származékai (például a trifluor-metanszulfonikus anhidrid és a trifluor-metanesul-klorid) kulcsfontosságú reagensek a trifluor-metil (- CF ∝) bevezetésében. A trifluor -metil (χ =4.0) erős elektronegativitása jelentősen megváltoztathatja a molekuláris polaritást, fokozhatja a gyógyszer stabilitását és a membrán permeabilitását. A tipikus alkalmazások a következők:
Antivirális gyógyszerek szintézise: A Remdesivir szintézisében a trifluor -metanesulfonikus anhidridet használják a nukleozid közbenső termékek aktiválására, a trifluor -metil erősen szelektív bevezetésének elérésére, és növelik a gyógyszerek gátló aktivitását az RNS vírus polimeráz RNS -vírus polimerázra.
Fluortartalmú peszticidek kialakulása: Köztes szintézis katalizátorként a herbicid szulfoxastrobin,trifluor -metanszulfonsavlerövidítheti a reakcióútot, növeli a teljes hozamot 45% -ról 78% -ra, és csökkentheti a termelési költségeket.


3. A szuperacid rendszer felépítésének sarokköve
A TFMSA szuperacid komplexeket képezhet (például H [CF ∝ SO ∝ bf ∝]), ha Lewis savakkal (például BF ∝, PF ₅) kombinálják, amelyek 10 ⁴ -szer erősebbek, mint a tiszta TFMSA. Az ilyen típusú komplex kiemelkedő teljesítményt mutat a következő területeken:
Szén szén -dioxid -kötés aktiválása: Az inert szén -szénkötések törésének katalizálása és a komplex molekulák szerkezeti átrendeződésének elérése. Például a ciklohexán benzolmá történő átalakításának hozama a hagyományos módszerek 5% -áról 35% -ra nőtt.
Királis katalízis: a királis ligandumokkal kombinálva az aszimmetrikus szintézis katalizátorok kialakulásához. Például a Ytterbium -trifluor -metanszulfonát (YB (OTF) ∝) által katalizált diel -reakciók 99% -os enantioszelektivitás (EE érték), és kulcsfontosságú királis közbenső termék a paklitaxel antikancer gyógyszer szintéziséhez.
1. Nukleozid vírusellenes gyógyszerek
Kettős szerepet játszik a nukleozid -analóg szintézisben:
A glikozid -kötés aktiválása: katalizátorként elősegíti a ribóz és a bázis kondenzációját. Például az anti -HIV -gyógyszer zidovudin (AZT) szintézisében ez tízszer növelheti a glikozidkötés képződésének sebességét, miközben gátolja az izomerek képződését.
Védelmi csoport eltávolítása: A védelmi csoportok, például a benzil -oxi -karbonil (CBZ) hatékony eltávolítása enyhe körülmények között, szenzoros csoportok károsodása nélkül. Például a COVID-19 gyógyszer-molnupiravir szintézisében a TFMSA katalitikus dotrotekciós lépésének hozama elérte a 92% -ot, ami jóval meghaladta a hagyományos hidrogenolízis lépés 65% -át.


2. A rákellenes gyógyszerek közbenső terméke
A TFMSA által katalizált reakciót széles körben használják a rákellenes gyógyszerek szintézisében:
Friedel Crafts Alkiláció: A gefitinib szintéziséhez a gefitinib szintéziséhez a legfontosabb köztitermék-4-fluor-fenilén-N-N-N-N-N-amin szintetizáltuk. A TFMSA katalízise alatt a reakcióidőt 24 óráról 4 órára rövidítették, és a hozam 50% -ról 85% -ra nőtt.
Aldehid -kondenzáció: Az imatinib szintézisében a TFMSA katalizálja az aldehidek és ketonok kondenzációját - hidroxi -ketonokat, amelyek kulcsfontosságú prekurzort biztosítanak az azt követő indolgyűrűk előállításához.
3. szteroidok és fehérje módosítások
Szteroid szintézis: A TFMSA katalizálja a szteroid szülőmagok hidroxilációs reakcióját, például a progeszteron 17 - hidroxi -progeszteron -ra történő átalakítását, a hozam a hagyományos módszerek 30% -áról 75% -ra és 99% regioszelektivitással nőtt.
Fehérje jelölése: Savas körülmények között stabil katalizátorként felhasználható a glikozid kötések specifikus hasítására a glikoproteinekben, segítve a fehérje -glikozilációs helyek elemzését. Például az antitest gyógyszerkonjugátumok (ADC) kifejlesztésében a kötőhelyek pontos lokalizációja javíthatja a gyógyszer célzását.

Anyagtudomány: A nagy teljesítményű anyagok molekuláris tervezői

1. A polimer anyagok módosítása
Szilikon gumi térhálósítás: A TFMSA katalizálja a szilikán kötéseket, javítva a szilikongumi hőállóságát és mechanikai szilárdságát. Például, a szilikon gumi szintézisében az űrrepülőgép alkalmazásokhoz, a TFMSA katalízissel térhálósított szilikon gumi hőmérsékletének hőmérséklete 300 fokról 450 fokra növekszik, és a szakítószilárdság megduplázódik.
Különleges műanyag szintézis: A ciklikus oligomerek katalitikus gyűrűnyílásának polimerizációja a magas hőmérsékleten és korrózió-rezisztens poliarileton (PAEK) és a poliimid (PI) előállításához. Például a TFMSA által katalizált polietereton (PEEK) szintézisében a molekulatömeg -eloszlási index (PDI) 2,5 -ről 1,2 -re csökkent, és az anyagfeldolgozási teljesítmény szignifikánsan javult.
2. nanomateriális sablonszer
Strukturális irányító szerként szabályozhatja a nanoanyagok morfológiáját és méretét:
Mezopórusos szilícium-dioxid: Az SBA-15 mezopórusos anyagok szintézisében a szilikátok öngyűjtését hidrogénkötés vezérli, hatszögletű mezopórusos szerkezetet képez, amely egyenletes pórusméretű (2-50 nm) és egy specifikus felület 1000 m ²/g. Ez alkalmas a gyógyszeres tartós kiadású hordozók számára.
Fém szerves keretek (MOF): katalizálja a ligandumok és a fémionok közötti koordinációs reakciót. Például a ZIF-8 szintézisében,trifluor -metanszulfonsavRövidítheti a kristályosodási időt 72 órától 6 óráig, és javíthatja a kristály tisztaságát 99%-ra.

Energia -technológiai mező: A zöld energia „kémiai gyorsítója”

1. Elektrolit lítium-ion akkumulátorokhoz
Nagyfeszültségű elektrolit: A lítium -trifluor -metanszulfonát (LIOTF) adalékanyagként javíthatja az elektrolit stabilitását 4,5 V feletti nagyfeszültségnél. Például a lítium -kobalt -oxid (LICOO ₂) katód anyagban az 5% -os LIOTF elektrolit hozzáadása az akkumulátor 500 ciklusának 500 ciklus után 70% -ról 85% -ra növelheti a kapacitás -visszatartási arányt.
Szilárd állapotú elektrolit interfész (SEI) szabályozás: A trifluor -metán -szulfonát részt vesz a SEI film kialakulásában, gátolja az elektrolit bomlását. Például a szilícium-alapú negatív elektródákban a LIOTF által katalizált SEI-film fluortartalma 30%-kal növekszik, és az akkumulátor első hatékonysága 75%-ról 88%-ra növekszik.
2. Üzemanyagcellás katalizátor
Protoncserélő membrán (PEM): A TFMSA-val módosított perfluoroszulfonsav gyanta (például NAFION) 50% -kal növekszik a proton vezetőképességében, és alacsony hőmérsékleten (-20 fok) képes fenntartani a hatékony vezetést, így alkalmassá teszi a jármű üzemanyagcelláira.
Az oxigén redukciós reakció (ORR) katalizátor: A TFMSA által segített platina -szén (PT/C) katalizátor, a platina részecskemérete 5 nm -ről 2 nm -re csökkent, a katalitikus aktivitás háromszorosára növekedett, és az üzemanyagcellák teljesítményének sűrűsége 1,2 W/cm ² -t ért el.
1. kipufogógázkezelő katalizátor
Illáló szerves vegyületek (VOC) oxidáció: A TFMSA -val módosított mangán -oxid -katalizátor teljes mértékben oxidálhatja a toluolt Co ₂ és H ₂ o -ra 150 fokos, a reakciósebességgel tízszer gyorsabb, mint a hagyományos katalizátorok.
A nitrogén -oxidok (NOX) csökkentése: A trifluor -metán -szulfonát elősegíti az aktív oxigénfajok képződését a réz alapú katalizátorok felületén. Oxigénben gazdag körülmények között az NOx N ₂ -re történő átalakításának hatékonysága eléri a 90%-ot, így alkalmas a dízel kipufogógáz kezelésére.


2. Adszorbensek a szennyvízkezeléshez
Nehézfém ion adszorpció: A TFMSA -val funkcionált mezopórusos szén anyag 200 mg/g és 150 mg/g adszorpciós kapacitása Pb ² ⁺ és Cd ² ⁺ esetén. Hatékonyan működhet savas körülmények között (pH =2), és alkalmas a gallinizáló szennyvízkezelésre.
Szerves szennyező anyagok lebomlása: A TFMSA által katalizált fotokatalitikus fenton reakció teljesen lebonthatja a festékeket, például a rodamin B látható fényben, ötször gyorsabb reakciósebességgel, mint a hagyományos Fenton módszer, és nincs vasiszap -előállítás.
1. Kvantumszámítási anyagok
Szuperacidként felhasználható topológiai szigetelők (például bi ₂ se ∝) és kétdimenziós anyagok (például grafén-oxid) előállítására, és felszíni állapot-ellenőrzési képessége új ötleteket nyújt a kvantumbitek kialakításához.
2. Biológiai képalkotó szondák
A TFMSA -val módosított fluoreszcens színezékek (például CY7 OTF) háromszoros növekedéssel bírnak a fotostabilitásban, és a sejtmembrán célzott képalkotást érhetik el a trifluor -metil hidrofób képessége révén, így alkalmassá teszik azokat a daganatok korai diagnosztizálására.
3. mezőgazdasági növény növekedési szabályozói
Növénynövekedési szabályozóként elősegítheti a gyökér fejlődését és a fotoszintézis hatékonyságát. Például a rizstenyésztés során a 0,1% TFMSA oldattal rendelkező lombpermetezés 15% -kal növelheti a hozamot, és jelentősen növeli a szállás ellenállását.

A kémia területén egyetemes eszközként alkalmazása áthatolta a modern technológia minden sarkát. Az alapvető reakció-katalízistől a legmodernebb anyagtervezésig, a gyógyszerészeti szintézistől a környezeti irányításig, az egyedi kémiai nyelv az interdiszciplináris innováció fejezetét írja.

Trifluor -metanszulfonsavelőször Haseldine és Kidd készítette 1954 -ben a következő módon:
Az IT ipari előkészítése a metanszulfonsav elektrokémiai fluorizálásán (ECF) történik:
Ch -ch3ÍGY3H + 4 HF → CF3ÍGY2F + H2O + 1.5H2
A CF3SO2F reakcióterméket hidrolizáljuk, hogy trifluor -metanszulfonát -ionot kapjunk. Ezenkívül az előkészítés trifluor -metilt is használhat szulfonil -klorid kezelésére, amelyet a reakciótermékből a következő hidrolízissel nyerünk:
CF3SCL + 2 Cl2 + 2H2O → CF3ÍGY2Oh + 4 hcl
A fenti módszerekkel előállított nyers terméket trifluor -metil -szulfon -anhidriddé történő desztillációval tisztíthatjuk.

A TFMSA egy erős szerves sav, amelyet általában a laboratóriumban használnak. Használható a trifluor -metanszulfonikus anhidrid és a különféle IT -származékok előállítására. Ez egy hatékony katalizátor az olefinek és az éterek oligomerizációjának és polimerizációjának.
Túlzott foszfor -pentoxid vagy vinil -keton jelenlétében dehidrációs reakción eshet át, hogy trifluor -metanesulfonikus anhidridet kapjon.
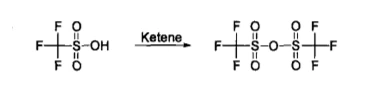
Ez az egyik legerősebb szerves sav. Az IT magas termodinamikai stabilitása és konjugált bázisának (trifluor -metanszulfonát) miatt nem érzékeny az általános redox reakciókra. Ezért sok sav-katalizált reakcióban felhasználható. Erős proton adományozó tulajdonsága miatt felhasználható néhány Diels-Alder ciklizációs reakció katalizálására, amelyek normál körülmények között nehéz előfordulni.

Trifluor -metanszulfonsavegy erős Lewis sav is, és a megfelelő trifluor -metanszul -szulil -csoport erős elektron abszorpciós tulajdonságokkal rendelkezik. Ha acilációs reagenssel kombinálják, aktivált acilációs közbenső terméket generál, amelyet könnyű katalizálni a Friedel-Crafts acilációs reakcióval. Például a trimetil-szilil-trifluor-metanszulfonát katalizálhatja a molekulán belüli Friedel-Crafts acilációs reakciót, hogy ciklikus ketonokat képezzen.

Az IT PKA -14,7 (± 2,0), amely a szerves szupersavhoz tartozik, és savassága meghaladja a 100% -os kénsavat.
Erős savassággal és redukálhatósággal rendelkezik. Általában szerves szintézis reagensként használják.
Amikor erős Lewis savak, például bór -trifluorid (BF3), a foszfor -pentafluorid és az arzén pentafluorid feloldódnak, a savasság erősebbé válik a stabil komplex savak képződése miatt: H3ÍGY3Bf3], H [vö.3ÍGY3PF5], H [vö.3ÍGY3Asf5].
Füst a levegőben, mert erős vízelnyeléssel rendelkezik, és könnyen reagálható a levegőben lévő nedvességgel, hogy stabil monohidrát CF -et képezzen3ÍGY3H · H2O, 34 fokos olvadási ponttal. Rendkívül oldódik a vízben, amely sok hőt enged fel.
Olvadási pont - 40 C fok, 162 C fokos C fok (lit.), sűrűség 1,696 g/ml 25 C fokon (lit.), gőz sűrűség 5,2 (vs levegő), gőznyomás 8 mm Hg (25 C fok), törésmutató n20/d 1.327 (lit.), RTECS szám: A +30 C fok alatt, oldhatóság H -ban, savasság együtthatója (PKA) - 14 (25 fokon), füstölgő folyadék képződése, specifikus gravitáció, kissé barna, pH -érték<1 (H2O), Water solubility SOLUBLE, Sensitivity
Népszerű tags: Trifluorometanszulfonsav CAS 1493-13-6, Szállítók, gyártók, gyár, nagykereskedelem, vétel, ár, ömlesztett, eladó






