Tesamorelina humán növekedési hormont felszabadító faktor (GRF) 44 aminosav szekvenciájából áll. A hexenoil tirozinjának N--terminálisához kapcsolódik. A molekulaképlet: C221H366N72O67S. XC2H4O (x ≈ 7), CAS 901758-09-6 és CAS 218949-48-5, relatív molekulatömege (szabad bázis) 5135,9. Az analógok egy új növekedési hormon felszabadító faktor, amely nemcsak a normál növekedési hormon szekréciót állíthatja helyre a szervezetben, hanem csökkenti a zsigeri zsírszövet (ÁFA) növekedését, javítja a vérzsír-rendellenességeket és az életminőséget, valamint fenntartja a glükóz dinamikus egyensúlyát a szervezetben. A gyógyszert az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága 2010 novemberében hagyta jóvá a HIV-vel kapcsolatos zsíranyagcsere-zavar szindróma kezelésére. Eladó tesamorelin peptidünk, de meg kell jegyezni, hogy a Shaanxi BLOOM Tech Co., Ltd. termékei kizárólag laboratóriumi használatra szolgálnak.
Termékeink



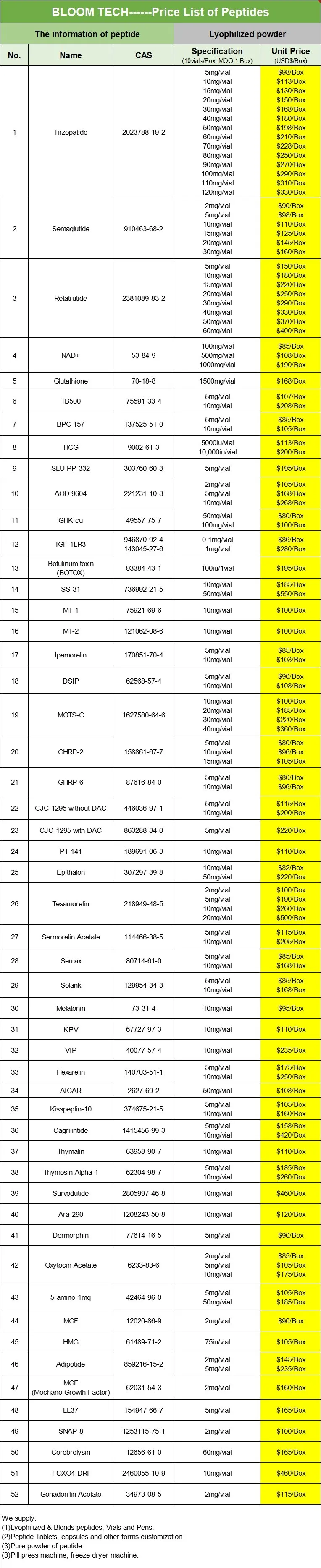
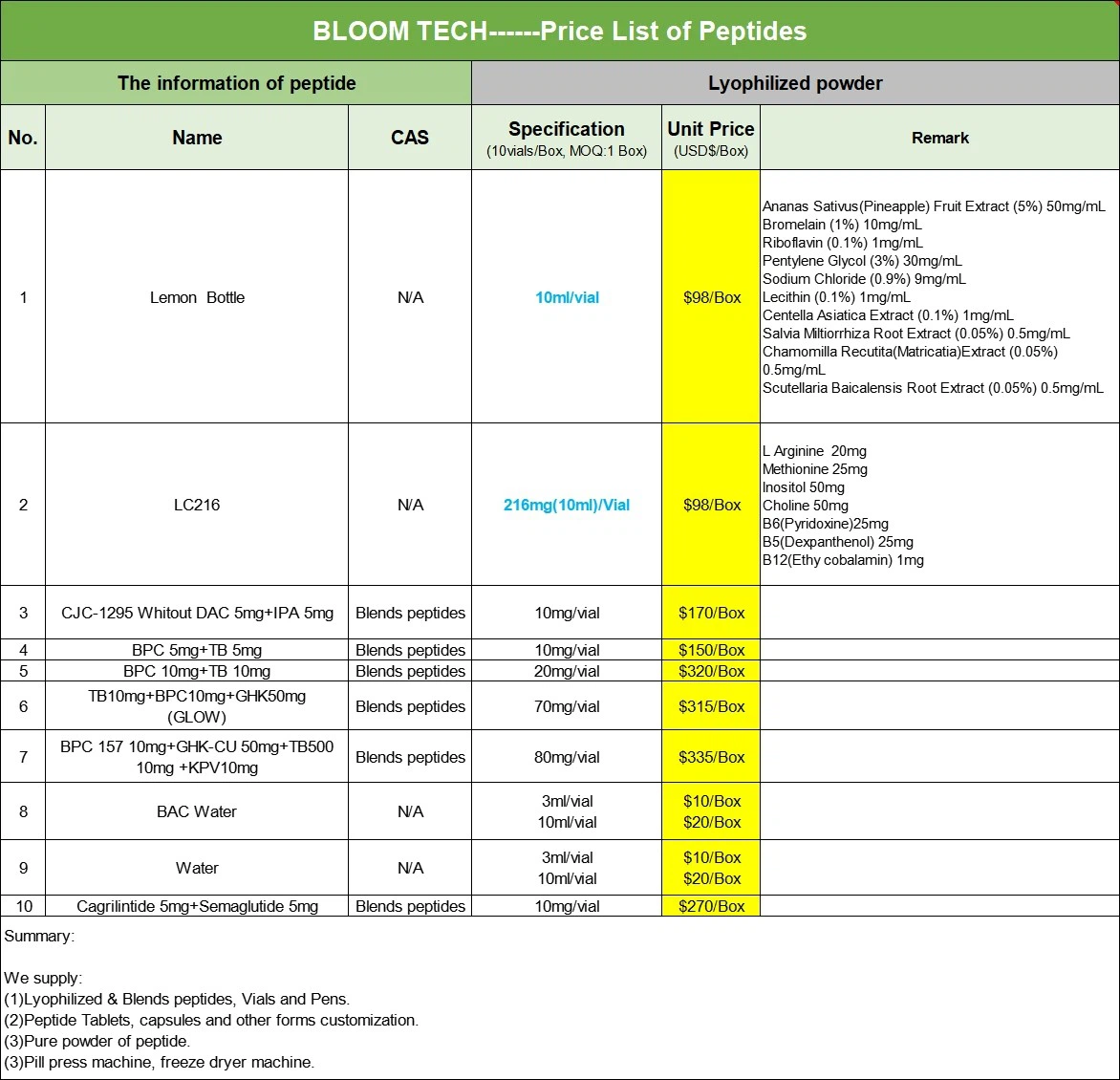


Tesamorelin COA


A fordított fázisú, nagy teljesítményű folyadékkromatográfiás tisztítási módszer a következő lépéseket tartalmazza:
1) A szilárd fázisú szintézisből nyert timorelin durva bőrt ionmentesített vízben oldjuk, és az állófázis egy fordított fázisú szilikagél oszlop tetraalkil-szilán kötésű szilikagéllel, oktaalkil-szilán kötésű szilikagéllel vagy oktadecil kötésű szilikagéllel, ahol a mobil fázis a két fázis, a szilikagél a foszfát pufferoldat az A fázis, a kromatogram tiszta acetonitril pedig a B fázis, és gradiens elúciós tisztítást végzünk a megcélzott csúcs bőroldatának összegyűjtésére.
2) A kapott oldatot vákuum rotációs bepárlóval betöményítjük, és a tömény oldatot készenléti üzemmódra fenntartjuk.
3) Használjon anioncserélő gyantát a cseréhez és alakítsa át hűtőközegmé
4) A végső nagy-tisztaságú kortizon oldatot koncentráljuk, és fagyasztva{2}}szárítjuk dekompresszióval, forgatással és ismételt bepárlással, így porszerű készterméket kapunk.
Ez a módszer alkalmas a temorelin ipari tisztítására. Nemcsak 98,0%-nál nagyobb tisztaságú finomított bőrt tud készíteni, hanem tételekben is előállítja, hogy megfeleljen a nagy tisztaság, a nagy hozam, az alacsony költség és a nagy hatékonyság követelményeinek.

Szintézis módszer
|
|
|
|
|
Az A peptidgyantát úgy állítottuk elő, hogy az Fmoc{0}}Leu-OH-t és más védő aminosavakat egy gyantával, mint hordozóanyaggal egymás után kapcsoltuk a temorelin sorrendjében.
A teljes védőfragmens B1-Bn (n egy egész szám, amely 2 kisebb vagy egyenlő, mint n<21) was synthesized by solid phase synthesis method respectively. The sequence of the fragments is part of the sequence of temorelin, and the sequence of total amino acids after connecting A and B1-Bn is the same as that of temorelin
Az A peptidgyantát egymás után kapcsoltuk a teljes -védőfragmenssel B1-Bn és a transz-hexénsavval a szilárd fázison, hogy megkapjuk a temorelin peptid gyantát.
Temorelin peptid gyanta pirolízise nyers peptid előállítására. A temorellin előállítási módszere könnyen kezelhető, alacsony költséggel, egyszerű tisztítással és magas hozammal
A kutatástörténet a HIV-vel (Human Immunodeficiency Virus) összefüggő zsíranyagcsere-zavarok kezelésével foglalkozik. Az alábbiakban néhány kulcsfontosságú pontot olvashat a kutatás történetéről:
1. Előzetes megállapítások
A HIV-fertőzött{0}}betegpopulációban egyes gyógyszerek károsíthatják a zsíranyagcserét a kezelés során, különösen a hasi zsír túlzott felhalmozódását. Ez a változás nemcsak a betegek fizikai megjelenését érinti, hanem az anyagcsere-rendellenességek és a szív- és érrendszeri betegségek fokozott kockázatával is összefüggésbe hozható. Ezért a kutatások fontos irányává vált olyan gyógyszerek keresése, amelyek hatékonyan kezelhetik ezt a zsíranyagcsere-zavart.
2. A hatásmechanizmus tanulmányozása
A növekedési hormon (GH) felszabadulásának szabályozása a szervezetben az emberi növekedési hormon felszabadító hormon (GHRH) hatásának utánzásával és fokozásával. A növekedési hormon kulcsszerepet játszik a testszövetek növekedésének, szintézisének és anyagcseréjének szabályozásában, és az agyalapi mirigyben található GHRH receptorhoz kötődve serkenti a növekedési hormon szekrécióját, ezáltal növeli a GH szintjét a szervezetben. Ez a felfedezés elméleti alapot nyújt a HIV-vel{2}}összefüggő lipidanyagcsere-zavarok kezeléséhez.Tesamorelin.
3. Klinikai vizsgálatok
A hatásmechanizmus alapján a kutatók számos klinikai vizsgálatot végeztek, hogy értékeljék a HIV-vel{0}}összefüggő diszlipidémia kezelésében való hatékonyságát. Ezek a vizsgálatok kimutatták, hogy a kezelés jelentősen csökkenti a hasi zsír felhalmozódását, és hatékonyan javítja a betegek zsírvesztési tüneteit. Ez pozitív hatással lehet a betegek pszichés és fizikai egészségére egyaránt.
4. FDA jóváhagyás
E klinikai vizsgálatok pozitív eredményei alapján ezt (Tesamorelin-acetát só, kereskedelmi név Egrifta) az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hatósága (FDA) 2010-ben engedélyezte a HIV-vel összefüggő zsíranyagcsere-zavarok kezelésére. Ez volt az első gyógyszer, amelyet az FDA jóváhagyott a lipidanyagcsere-zavarok kezelésére.
Összefoglalva a történeteTesamorelina kutatások egyike a lehetséges terápiás hatások felfedezése, a hatásmechanizmusok mélyreható-feltárása, a hatékonyság klinikai vizsgálatokon keresztül történő validálása, és végső soron a hatósági jóváhagyás. Ennek a folyamatnak a sikere nemcsak új terápiás lehetőséget kínál a HIV-fertőzött-betegek számára, hanem új ötleteket kínál a zsíranyagcsere-zavarokhoz kapcsolódó egyéb rendellenességek kezelésére is.
|
|
|
|
A tesamorelin gátolja a GSK-3-at és csökkenti a tau fehérje foszforilációját az IGF-1-en keresztül
A tesamorelin egy mesterségesen szintetizált növekedési hormon-felszabadító faktor (GHRH) analóg, amely serkentheti a növekedési hormon (GH) szekrécióját az agyalapi mirigy elülső részéből, ezáltal befolyásolva az inzulin{0}}szerű növekedési faktor-1 (IGF-1) szintjét. Az elmúlt években a kutatások azt találták, hogy a Tesamorelin szabályozhatja a tau fehérje foszforilációját az IGF-1-hez kapcsolódó jelátviteli útvonalakon keresztül, új reményt hozva a neurodegeneratív betegségek kezelésében.
A GSK-3 jellemzői és kapcsolata a tau fehérje foszforilációjával
A GSK-3 szerkezete és enzimatikus jellemzői
A glikogén szintáz kináz-3 (GSK-3) egy szerin/treonin protein kináz, amely széles körben jelen van a sejtekben. A GSK-3 egyedi szerkezeti jellemzőkkel rendelkezik, és aktivitását számos tényező szabályozza. Nyugalomban a GSK-3 bizonyos alapaktivitással rendelkezik, és aktivitása tovább fokozódik, ha upstream jelek aktiválják. A GSK-3 szubsztrátok széles skálájával rendelkezik, és különféle fehérjéket képes foszforilálni, különböző jelátviteli útvonalakban és fiziológiai folyamatokban részt venni a sejten belül.
Tau fehérje foszforilációja GSK-3 által
A Tau fehérje egy mikrotubulusokhoz kapcsolódó fehérje, amely főként a neuronok mikrotubulusainak összeállításában és stabilitásában vesz részt. A tau fehérjén több foszforilációs hely található, és a GSK-3 az egyik fő kináz, amely katalizálja a tau fehérje foszforilációját. A GSK-3 specifikusan képes felismerni és foszforilálni a tau fehérje specifikus szerin- és treoninmaradékait, mint például a Ser396, Thr231 stb. A tau fehérje túlzott foszforilációja a mikrotubulusokhoz való kötődési képességének csökkenéséhez, a mikrotubulusok szerkezetének megzavarásához vezethet, ami viszont befolyásolja az anyagszállítást, a neuronok végső halálát és normális működését.
A GSK-3 szerepe a neurodegeneratív betegségekben
Az olyan neurodegeneratív betegségekben, mint az AD, a GSK-3 aktivitása abnormálisan megnövekszik, ami szorosan összefügg a tau fehérje túlzott foszforilációjával és a neurofibrilláris gubancok kialakulásával. A kutatások kimutatták, hogy a GSK-3 aktivitásának gátlása csökkentheti a tau fehérje foszforilációs szintjét, javíthatja a neuronális patológiás változásokat és késlelteti a betegség progresszióját. Ezért a GSK-3 a neurodegeneratív betegségek kezelésének egyik fontos célpontjává vált.
A Tesamorelin IGF-1 szekréciót stimuláló mechanizmusa
Lorem ipsum dolor sit amet consectetur
Kölcsönhatás a Tesamorelin és a GHRH receptor között
A tesamorelin, mint GHRH analóg, specifikusan kötődhet az agyalapi mirigy elülső sejtek felszínén lévő GHRH receptorokhoz. Ennek a kötődésnek nagy affinitása és specifitása van, hasonlóan a természetes GHRH és a receptorok közötti kölcsönhatáshoz. Amikor a Tesamorelin a GHRH receptorhoz kötődik, konformációs változást okoz a receptorban, aktiválva a sejten belül a G-fehérjéhez kapcsolt jelátviteli útvonalat.
Az intracelluláris jelátviteli utak aktiválása
Miután a Tesamorelin a GHRH receptorokhoz kötődik, az aktivált G-fehérje tovább aktiválja az adenilát-ciklázt (AC), ami az intracelluláris ciklikus adenozin-monofoszfát (cAMP) szintjének növekedéséhez vezet. A CAMP, mint másodlagos hírvivő, aktiválja a protein-kináz A-t (PKA). A PKA különféle downstream célfehérjéket foszforilálhat, beleértve a transzkripciós faktorokat is, ezáltal elősegítve a GH gének transzkripcióját és expresszióját, ami végső soron a GH szekréció növekedéséhez vezet.
Az IGF-1 szintézis indukálása GH által
A véráramba szekretált GH olyan szövetekre hat, mint a máj, aktiválva a JAK-STAT jelátviteli útvonalat a májsejteken belül, hogy elősegítse az IGF-1 gén transzkripcióját és expresszióját. A májsejtek felszínén lévő GH receptorokhoz való kötődés után a GH aktiválja a receptorhoz kapcsolódó JAK kinázokat, amelyek tovább foszforilálják a STAT fehérjéket. A foszforilált STAT fehérjék dimereket képeznek, belépnek a sejtmagba, kötődnek az IGF-1 gén promoter régiójához, és elindítják az IGF-1 szintézisét és szekrécióját.
Az IGF-1 gátolja a GSK-3 aktivitás jelátviteli útvonalát
Az IGF-1 receptor aktiválása
Miután az IGF-1 kiválasztódik a véráramba, a célsejtek felszínén lévő IGF-1 receptorhoz (IGF-1R) kötődik. Az IGF-1R egy tirozin-kináz receptor. Amikor az IGF-1 a receptorhoz kötődik, konformációs változást okoz, és aktiválja a receptor tirozin kináz aktivitását. Az aktivált IGF-1R önmagában foszforilálja és foszforilálja a downstream jelátviteli molekulákat, például az inzulinreceptor szubsztrát (IRS) fehérjéket.
A PI3K Akt jelátviteli útvonal aktiválása
A foszforilált IRS fehérjék képesek toborozni és aktiválni a foszfatidil-inozitol 3-kinázt (PI3K). A PI3K katalizálja a foszfatidil-inozitol-3,4,5-trifoszfát (PIP3) képződését a foszfatidil-inozitol-4,5-difoszfátból (PIP2) a sejtmembránon. A PIP3, mint másodlagos hírvivő, képes toborozni a protein-kináz B-t (Akt) a sejtmembránra és aktiválni azt. Az aktivált Akt egy kulcsmolekula, amely gátolja a GSK-3 aktivitását.
Az Akt gátló hatása a GSK-3-ra
Az Akt közvetlenül képes foszforilálni a GSK-3 specifikus szerin-maradékait (például Ser9), és a foszforilált GSK-3 aktivitása gátolt. Ez a gátló hatás megakadályozza, hogy a GSK-3 foszforilálja a szubsztrátokat, például a tau fehérjét, ezáltal csökkenti a tau fehérje abnormális foszforilációs szintjét.
A GSK-3 aktivitás gátlásának hatása a tau fehérje foszforiláció szintjére
In vitro kísérleti kutatás
In vitro sejtkísérletek során a kutatók az idegsejteket tesamorelin vagy IGF-1 környezetnek tették ki, majd megmérték a tau fehérje foszforilációs szintjét. Az eredmények azt mutatták, hogy Tesamorelinnal és IGF-1-gyel végzett kezelés után a GSK-3 aktivitása szignifikánsan csökkent az idegsejtekben, és a tau fehérje foszforilációs szintje is jelentősen csökkent több foszforilációs helyen. Ez azt jelzi, hogy a Tesamorelin az IGF-1-Akt jelátviteli útvonalon keresztül gátolja a GSK-3 aktivitást, hatékonyan csökkentve a tau fehérje foszforilációját.
Állatkísérleti kutatás
Állatmodellekben, például transzgenikus AD egérmodellekben a Tesamorelinnal végzett kezelést követően az egér agyszövetében megnőtt az IGF-1 szintje, a GSK-3 aktivitás gátolt, és a tau fehérje foszforilációs szintje csökkent. Ezzel egyidejűleg javult az egerek kognitív funkciója, és csökkent az idegsejtek károsodása. Ezek az állatkísérleti eredmények tovább erősítik a Tesamorelin mechanizmusának hatékonyságát a GSK-3 gátlásában és az IGF-1-en keresztüli tau protein foszforiláció csökkentésében in vivo.
GYIK
1. Kérdés: A Tesamorelin alkalmazható-e a nem-HIV-vel- kapcsolatos zsigeri zsírfelhalmozódásra? Mik a jelenlegi adatok?
Válasz: Bár a Tesamorelint jelenleg csak az FDA hagyta jóvá a HIV-vel kapcsolatos zsigeri zsírfelhalmozódás kezelésére, kis{0}}léptékű tanulmányok tárták fel a zsigeri elhízás egyéb okaira (például metabolikus szindróma, nem-alkoholos zsírmájbetegség) gyakorolt hatásait. Az előzetes adatok arra utalnak, hogy csökkentheti a zsigeri zsír mennyiségét és javíthatja az inzulinérzékenységet is, de a hosszú távú hatékonyságot és biztonságosságot a mérvadó intézmények nem ismerték el. Érdemes megjegyezni, hogy a hatásmechanizmusa (növekedési hormon{5}}felszabadító hormon analógja) elméletileg a zsigeri zsír túlzott felhalmozódásának bármely okára vonatkozik, de ez "felhasználásnak" minősül, és a kezelés költsége rendkívül magas (akár évi 30 000 dollár felett), ami korlátozza a kapcsolódó kutatások kiterjesztését.
2. K: Vannak-e speciális követelmények a Tesamorelin injekció beadásának helyére? Miért javasolt a hasi injekció a klinikai gyakorlatban?
V: A klinikai ajánlás szerint a has bőre alá kell beadni az injekciót (elkerülve a köldök körüli 5 centiméteres területet), és ez nem véletlenszerű választás. A korai farmakokinetikai vizsgálatok azt találták, hogy a combba vagy a karba adott injekcióhoz képest a gyógyszer felszívódása stabilabb, és a helyi mellékhatások (például bőrpír, duzzanat és keményedés) előfordulása valamivel alacsonyabb. Ez összefügghet a hasi bőr alatti zsír vérellátásával és szövetsűrűségével. Ezenkívül az injekció beadásának helyét váltogatni kell a zsíros alultápláltság (atrófia vagy hiperplázia) elkerülése érdekében, ami különösen fontos a kóros zsíreloszlású HIV-betegek számára.
3. K: A Tesamorelin hosszú távú-használata befolyásolja a saját növekedési hormon (GH) szekréciós ritmusát, vagy visszacsatolás gátlásához vezet?
A: There is a theoretical risk, but the existing clinical data (with the longest study lasting approximately 2 years) do not show that Tesamorelin causes definite GH axis feedback inhibition or permanent secretion disorder. As a growth hormone-releasing hormone (GHRH) analogue, it mimics physiological pulse stimulation and is more likely to maintain the rhythmicity of GH secretion compared to direct exogenous growth hormone supplementation. However, after discontinuation, visceral fat usually returns to the pre-treatment level within several months, suggesting that its effect is "reversible regulation" rather than a cure. The long-term impact on the hypothalamic-pituitary axis has not been sufficiently studied in the population using it for ultra-long-term use (>5 év).
4. Kérdés: Melyek a Tesamorelin szintézisének és a polipeptid tisztaságának specifikus kihívásai? Miért nehezebb a generikus gyógyszerek fejlesztése?
Válasz: A Tesamorelin egy szintetikus peptid, amely 44 aminosavból áll. Előállítása két ritka nehézségbe ütközik:
Stabilitási probléma: A peptidlánc hajlamos az oxidációra vagy hidrolízisre, különösen a tirozin az 1. pozícióban és az amid C-terminális a 44. pozícióban. Ez rendkívül szigorú feltételeket igényel a gyártási folyamatok (például szilárd-fázisú szintézis, tisztítás és fagyasztva{5}}szárítás) tekintetében.
Immunogenitási kockázat: Még kisebb szekvenciahibák vagy szennyeződések (például csonka peptidek) is kiválthatják az antitestek termelődését, potenciálisan semlegesítve az endogén GHRH-t vagy csökkentve a hatékonyságot. Az eredeti gyógyszer szabályozza a szennyeződés tartalmát<0.1% through proprietary purification technology, while generic drugs need to prove bioequivalence not only in terms of pharmacokinetics but also in terms of immunogenicity characteristics, which increases the development barrier.
Népszerű tags: tesamorelin cas 218949-48-5, beszállítók, gyártók, gyár, nagykereskedelem, vétel, ár, ömlesztve, eladó